IF 14.1!巨噬细胞和血小板药细胞结合递送系统促进脊髓损伤后的再生
QQ学术交流群:1092348845
详细介绍
本文精选
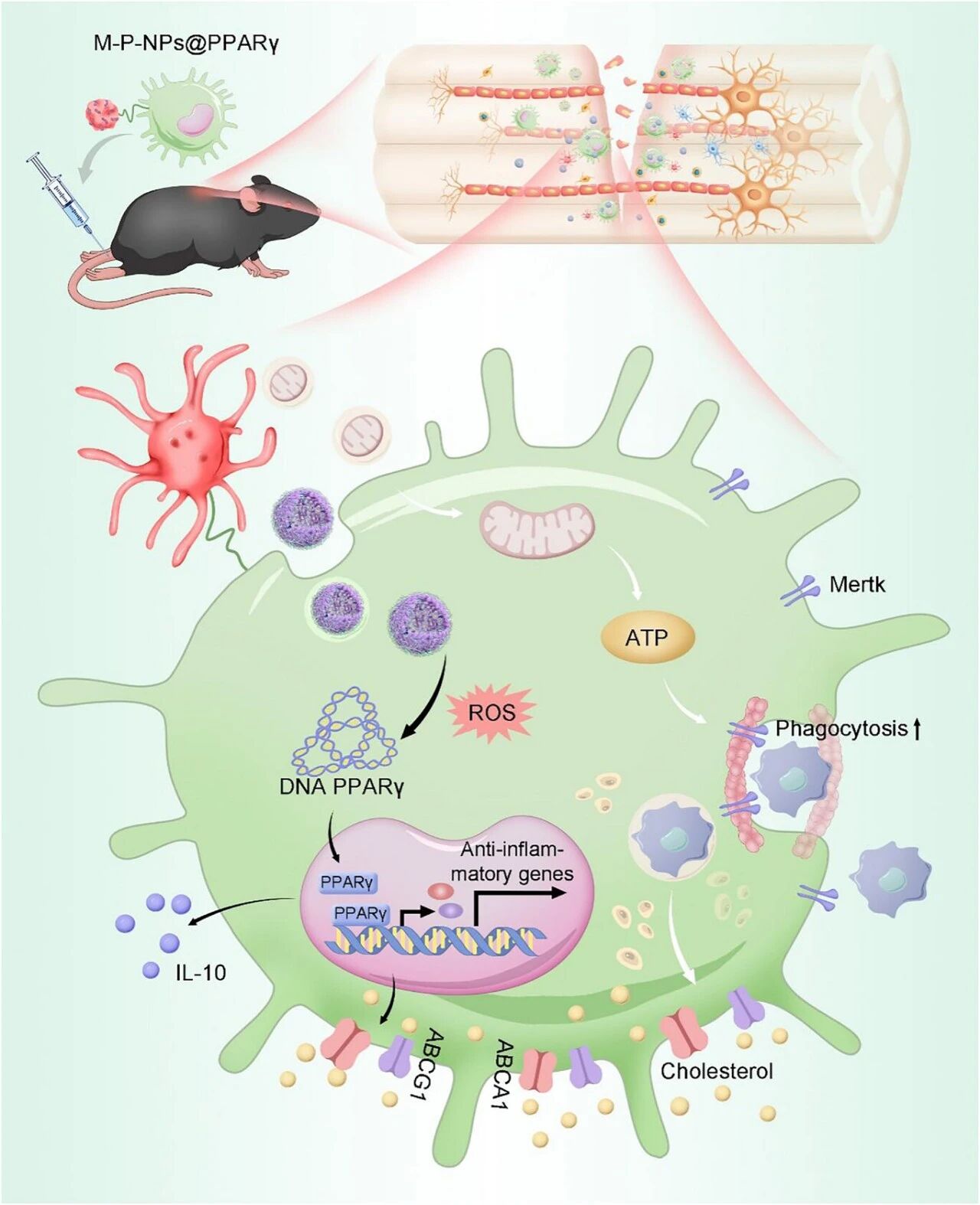
线粒体功能障碍常见于胞葬作用缺陷的巨噬细胞中,这种障碍会阻碍组织损伤的恢复。靶向细胞间线粒体转移是增强细胞治疗潜力的一种前景广阔的策略。本研究阐明了无核血小板线粒体的抗应激能力,并证明血小板在细胞应激状态下可将线粒体转移至巨噬细胞,从而恢复其受损的胞葬功能。本研究设计了一种递送系统:将负载阳离子聚合物纳米颗粒(NPs)用于过表达PPARγ的血小板与巨噬细胞偶联(M-P-NPs@PPARγ)。在该系统中,活化血小板可诱导线粒体转移并将NPs释放至巨噬细胞内,从而提升ATP生成并维持脂质稳态。以胞葬功能缺陷的代表性中枢神经系统疾病――脊髓损伤模型为概念验证,M-P-NP@PPARγ能够逆转受损的胞葬作用,进而促进神经再生与髓鞘修复,最终推动运动功能恢复。综上所述,本研究开发了一种结合线粒体与基因递送的策略,通过调控能量与脂质代谢来恢复损伤后巨噬细胞的胞葬功能。
创新点
1.本研究首次提出并验证了无核血小板作为线粒体供体的独特抗应激优势,突破了传统有核细胞来源线粒体在转移效率与稳定性方面的局限,为细胞器移植领域提供了新的来源选择。
2. 研究创新性地构建了“血小板-巨噬细胞”偶联递送系统,将线粒体转移与基因纳米颗粒(NPs)递送相结合,实现了对巨噬细胞能量代谢(ATP生成)与脂质代谢(PPARγ调控)的双重协同调控,从多维度纠正胞葬功能障碍。
3. 该工作将基础的线粒体转移现象,转化为一种具有明确分子设计(M-P-NPs@PPARγ)的治疗策略,并在复杂的脊髓损伤模型中证实其能通过恢复胞葬作用促进神经再生,为中枢神经系统损伤修复提供了兼具机制深度与应用潜力的新方案。
思路延伸
1.可探索该策略在其他与胞葬功能障碍或巨噬细胞代谢失调密切相关疾病中的应用潜力,例如动脉粥样硬化、纤维化疾病或神经退行性疾病,研究线粒体支持与代谢重编程能否在不同病理背景下普遍改善巨噬细胞功能并缓解组织损伤。
2.可对递送系统进行进一步优化,例如筛选更高效的线粒体供体细胞或改造策略,开发能响应特定疾病微环境信号(如活性氧、特定酶)而触发线粒体释放的智能型血小板载体,以提升治疗的时空精准性与安全性。
3.可深入探究线粒体转移后巨噬细胞内具体的代谢重编程路径与表观遗传改变,阐明线粒体输入如何通过影响乙酰辅酶A、活性氧等代谢物水平,进而调控与胞葬作用相关基因的表达网络,从机制层面建立更完整的“代谢-免疫功能”因果关系链。
原文链接
A Conjugation Delivery System of Macrophages and Platelet Pharmacytes Promotes Regeneration After Spinal Cord Injury
Advanced Science ( IF 14.1 )
Pub Date : 2025-12-25
DOI: 10.1002/advs.202513474
Haoli Wang, Hao Hu, Yijun Li, Lintao Hu, Chenhui Gu, Yiwei Zhu, Jing Huang, Na Li, Shuqi Jiang, Shouyan Zu, Jiachen Xu, Yining Wang, Ke Yang, Pengfei Chen, Liqing Shangguan, Yongcheng Wang, Shunwu Fan, Xianfeng Lin, Qingqing Wang
- 上一款: IF 19!笼状纳米药物通过协调内质网与线粒
- 下一款: ACS Nano | 通过利用超声激活纳米泡


 学术前沿
学术前沿