IF 14.1!具有双酶模拟活性的免疫调节纤维支架可防止术后肿瘤复发
QQ学术交流群:1092348845
详细介绍
本文精选
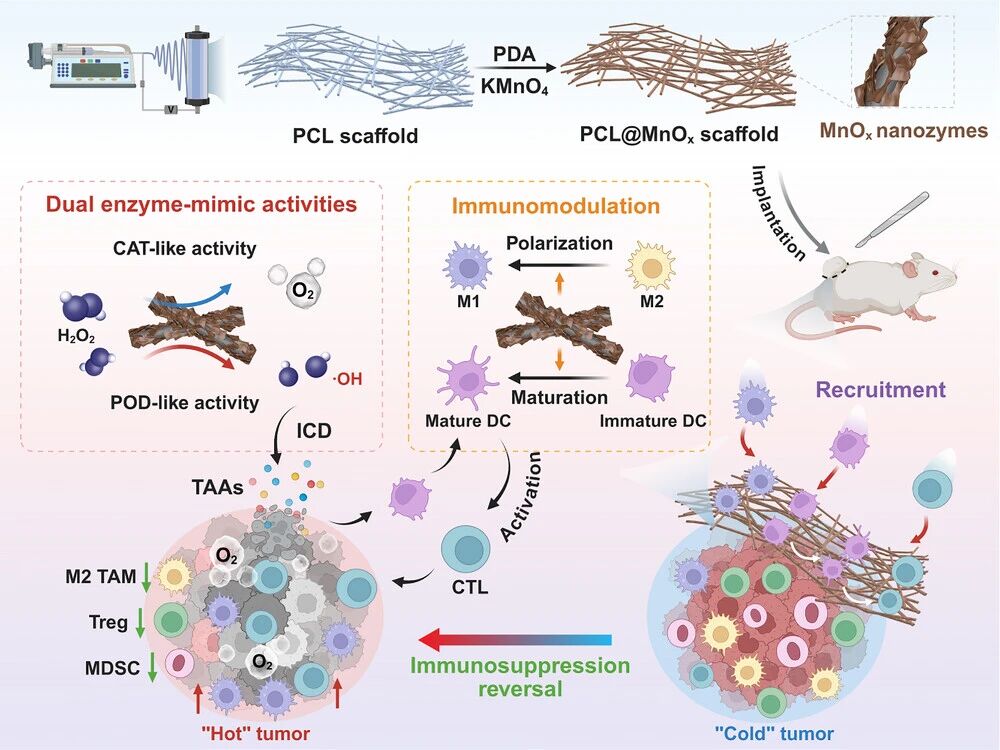
外科切除仍是实体瘤的一线治疗方案。然而,由残留肿瘤细胞和免疫抑制性微环境驱动的术后复发,持续挑战着患者的长期生存。本研究提出了一种功能化MnOx纳米酶的可植入纤维支架,用于预防肿瘤复发。MnOx纳米酶的双重模拟酶活性赋予该支架免疫调节功能。一方面,具有过氧化物酶样活性的MnOx纳米酶催化生成具有细胞毒性的羟基自由基,从而触发免疫原性细胞死亡和抗原释放。另一方面,其过氧化氢酶样活性通过分解H₂O₂生成O₂,有助于缓解缺氧,从而将巨噬细胞重编程为促炎的M1表型。同时,释放的Mn²⁺离子可作为有效的免疫佐剂,促进免疫细胞募集和活化。这种协同的免疫调节级联反应使支架能够建立一个持续存在的局部免疫微环境。体外和体内评估均证实,这种MnOx功能化支架能够引发强大的抗肿瘤免疫反应,无需外源性免疫刺激剂即可有效预防术后复发。这项工作凸显了一种基于材料的免疫治疗策略,它利用纳米酶固有的催化和免疫调节特性来设计用于术后癌症治疗的生物活性支架。
创新点
1.本研究创造性地将具有双重模拟酶活性的MnOx纳米酶集成于可植入纤维支架中,构建了一种兼具物理支撑与主动免疫调节功能的生物活性平台,超越了传统支架仅作为填充物或被动载体的局限。
2.该设计巧妙地利用单一纳米酶组分的过氧化物酶和过氧化氢酶样活性,协同触发免疫原性细胞死亡与改善肿瘤微环境缺氧,并将释放的Mn²⁺作为内源性佐剂,实现了无需外界添加细胞因子或药物的“自驱动”免疫级联激活。
3.研究系统阐明了从催化活性到免疫细胞重编程(如巨噬细胞向M1表型极化)再到抗肿瘤免疫记忆建立的完整机制链条,为术后局部免疫微环境的长期重建提供了一个闭环、可持续的材料学解决方案。
科研启发
1.该工作启发了“材料即治疗剂”的研发理念,表明通过精准设计材料的本征化学与催化属性(如纳米酶活性),可直接赋予植入器械强大的生物调控功能,从而简化治疗系统、降低安全风险。
2.它凸显了在肿瘤治疗中协调多个免疫环节(如直接杀伤、抗原释放、微环境重塑和免疫佐剂)的重要性,提示未来免疫工程策略需着眼于设计能够同步干预多个关键步骤的集成化平台。
3.本研究为探索其他具有生物活性的无机纳米材料(如基于铁、钴、铈的氧化物)在免疫调节中的应用提供了范式,鼓励科研人员深入挖掘材料本身固有的生物效应,而非仅将其视为惰性载体。
原文链接
Immunomodulatory Fibrous Scaffold with Dual Enzyme-Mimic Activities Prevents Postsurgical Tumor Recurrence
Advanced Science ( IF 14.1 )
Pub Date : 2025-12-27
DOI: 10.1002/advs.202519431
Xiaoyi Zhao, Zhuolong Jiao, Yue Wang, Huimeng Gu, Longfei Li, Jian Song, Chen Xu, Jiajia Xue, Fu‐Jian Xu, Nana Zhao
- 上一款: IF 19!异构碳涂层氮化碳空心纳米管,用于
- 下一款: Bioactive Materials|离子


 学术前沿
学术前沿