Advanced Materials | 肽诱导铁电在电荷转移超分子材料中
QQ学术交流群:1092348845
详细介绍
有机铁电材料在可持续能源转换、信息存储、柔性电子器件以及作为软植入体的潜在生物医学应用等领域具有重要价值。尽管应用前景广阔,但由于缺乏与无机体系相比成熟的设计策略,有机铁电材料的发展仍受局限,目前固态体系中已知的实例寥寥无几。受生物启发的超分子化学为构建可水加工且生物兼容的功能性纳米结构提供了新途径。本研究报道了一种超分子电荷转移体系:通过将肽链共价连接至电子给体-受体单元对,构建出可在水中自组装为纳米级带状结构的两亲分子。这些晶体纳米结构中肽链手性诱导的对称破缺不仅产生二次谐波活性,还在多种电荷转移体系中实现铁电行为,为设计新型有机铁电材料提供了普适性超分子策略。此外,在原代神经元细胞培养实验中,铁电材料涂层能促进轴突生长并增强动作电位,表明铁电纳米材料的极性结构有助于提升神经元成熟度。该超分子策略有望开发新型可水加工铁电生物材料,为细胞电荷转移、神经元轴突生长、肽对称破缺、自组装肽、超分子铁电体、细胞增殖及生物电子学等创新应用开辟道路。

该研究以题为“Peptide-Induced Ferroelectricity in Charge-Transfer Supramolecular Materials”发表在Advanced Materials上。
PowerPoint
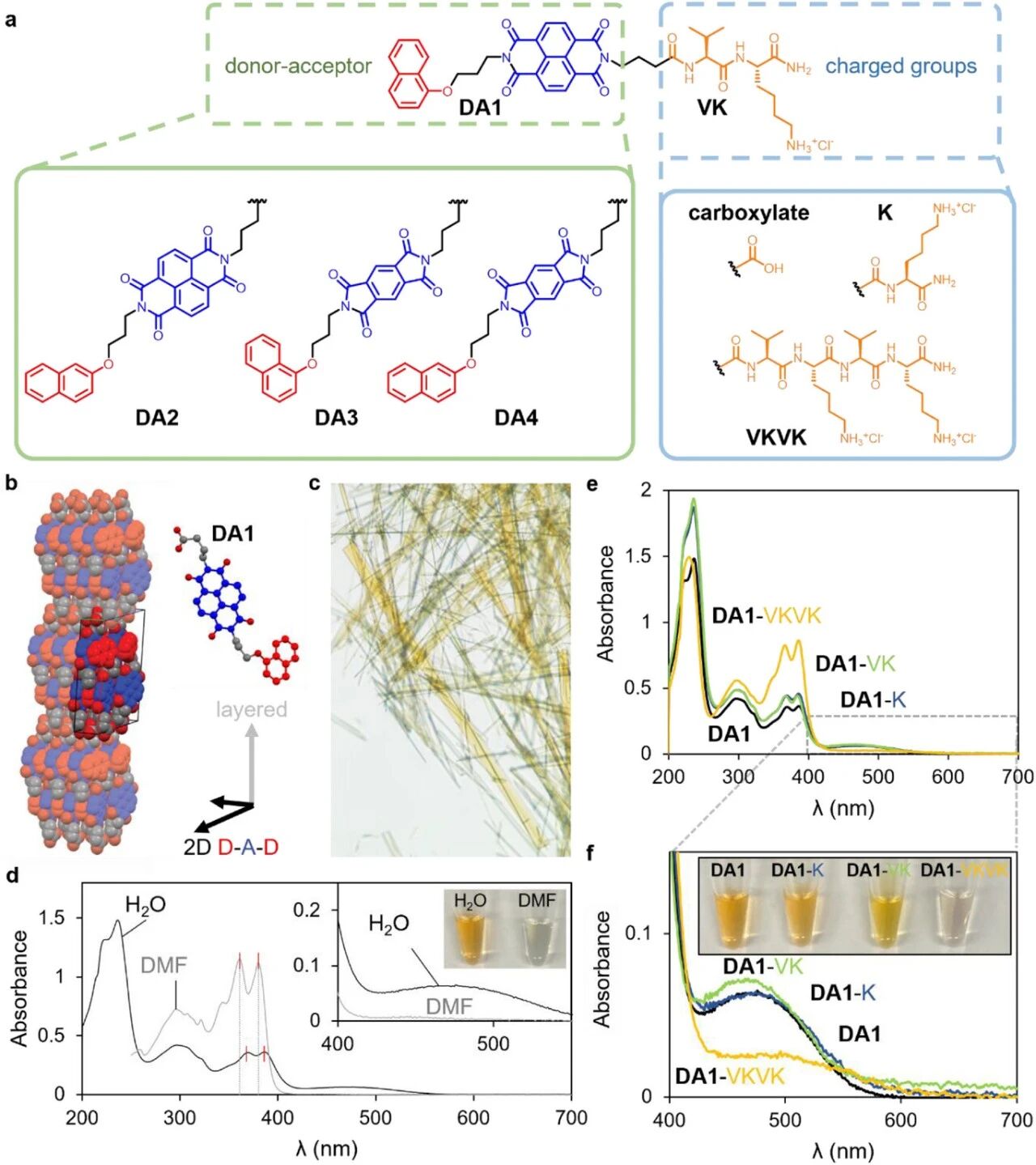
供体-受体肽两亲物的分子结构及自组装。a,DA-PAs的分子结构,包括通过三碳烷氧基连接子与PMDI或NDI受体相连的萘供体。受体单元通过三碳连接子与四种带电基团之一相连:羧酸盐、酰胺端赖氨酸(K)、酰胺端缬氨酸-赖氨酸(VK)或酰胺端四肽VKVK。b,通过DMSO缓慢蒸发获得的DA1单晶晶体结构(受体部分显示为蓝色,供体部分显示为红色,晶体形成层状结构,层内DA分子呈头尾排列,并形成供体-受体堆叠)。c,DA2晶体的照片(DA1晶体指标见图S4)。d,DA1溶于DMF(黑色曲线)或含1当量NaOH的水溶液(灰色曲线)的紫外-可见吸收光谱(插图为紫外-可见吸收光谱的电荷转移区域及1 mM水溶液和DMF溶液的照片)。e、f,含1当量NaOH的DA1水溶液、DA1-K、DA1-VK和DA1-VKVK的紫外-可见吸收光谱(e),以及e中电荷转移区域的放大光谱(f)(插图为1 mM水溶液的照片)。
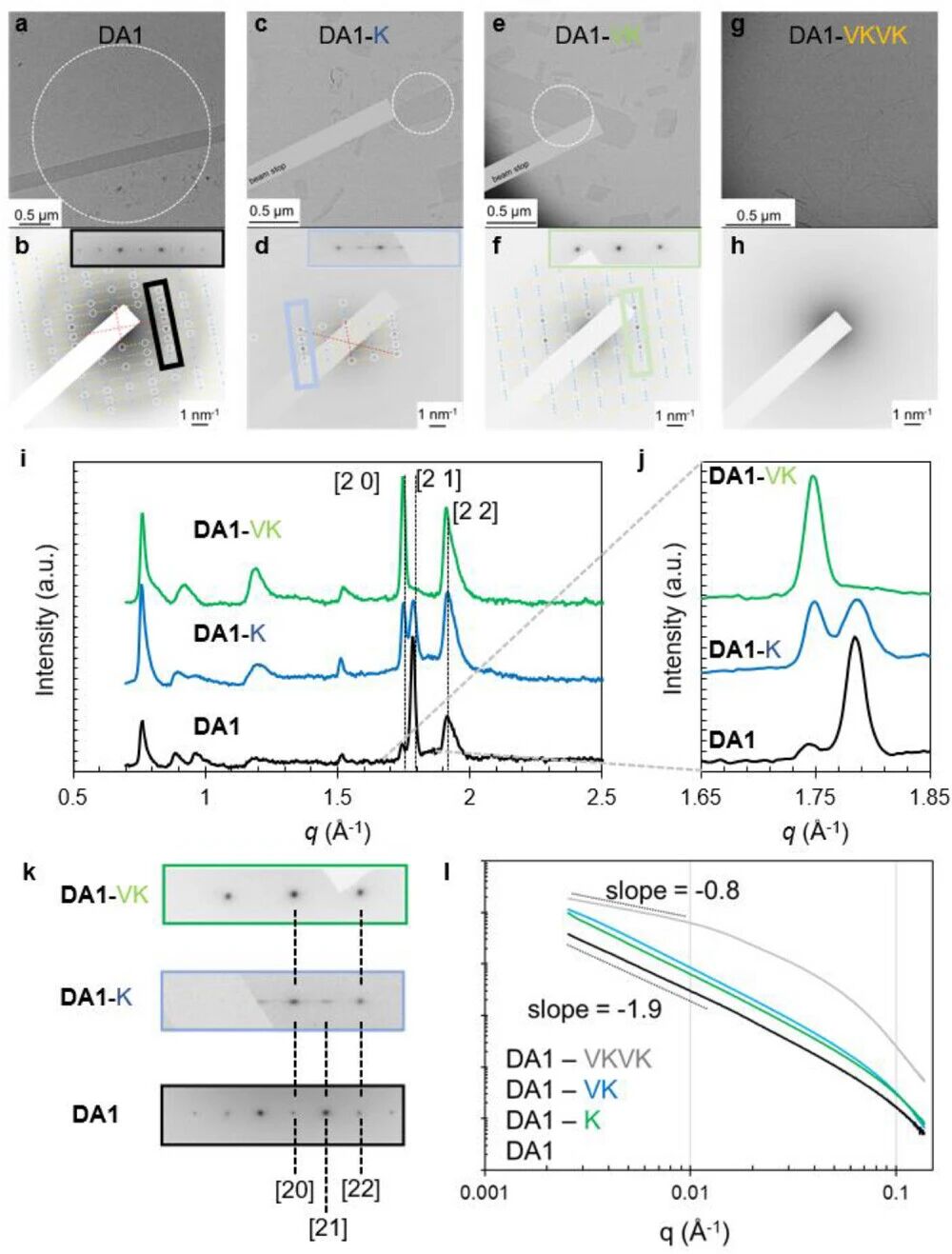
供体-受体肽两亲物的结构表征。a-h分别为DA1(a)、DA1-K(c)、DA1-VK(e)和DA1-VKVK(g)的透射电子显微照片;DA1(b)、DA1-K(d)、DA1-VK(f)和DA1-VKVK(h)的选区电子衍射图(白色虚线标示选区光阑,b、d和f插图为衍射图中相应彩色区域的放大图,红色虚线交叉点表示透射束位置)。i,j为含1当量NaOH的DA1水溶液、DA1-K及DA1-VK的广角X射线散射(WAXS)图谱,j中放大相关WAXS区域用于与电子衍射比对。k为从b、d、f中相应彩色框区域放大的SAED图。l为DA1-PA组装体水溶液(包括DA1黑色曲线、DA1-K绿色曲线、DA1-VK蓝色曲线和DA1-VKVK灰色曲线)的小角X射线散射(SAXS)图谱。
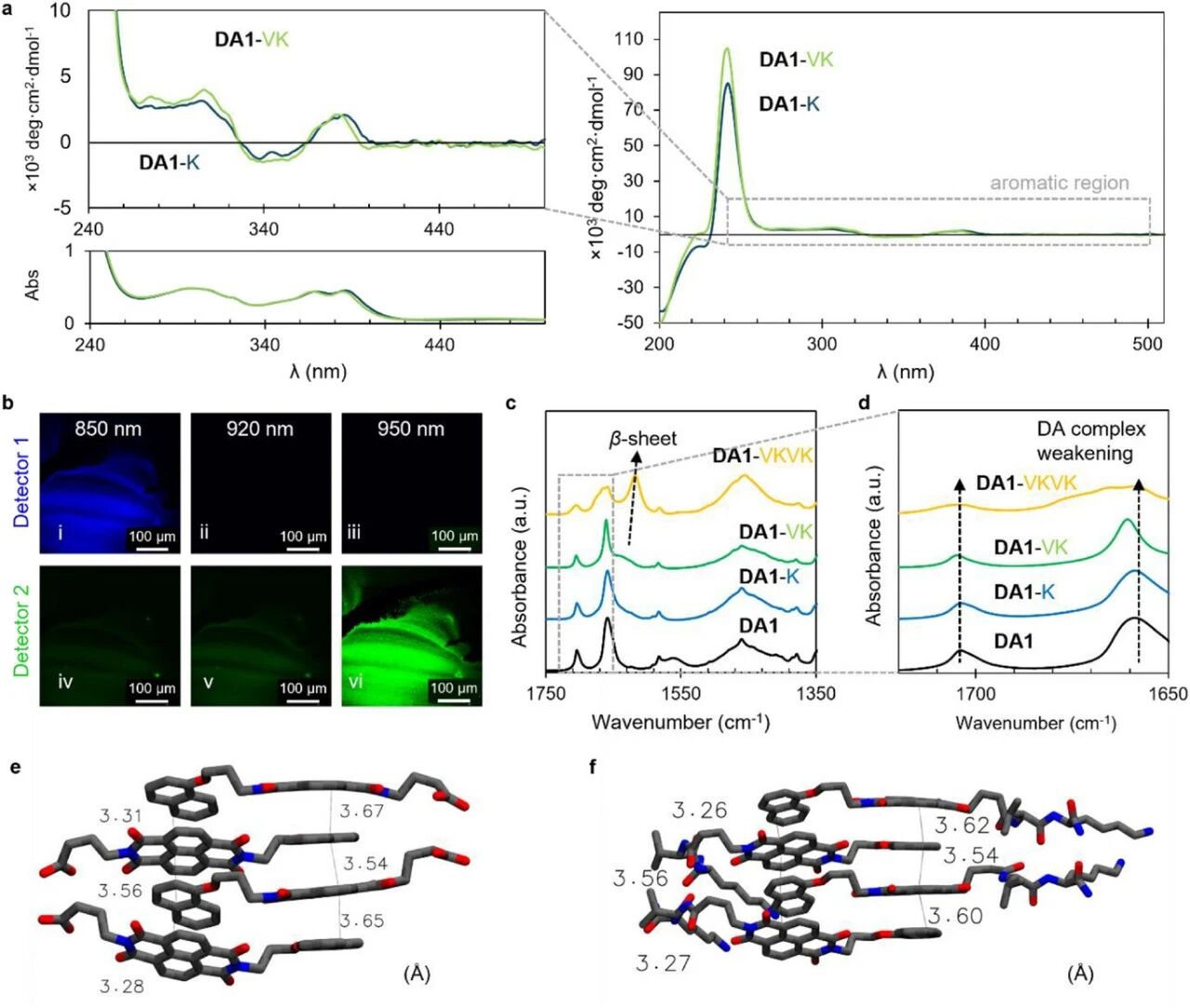
供体-受体肽两亲物晶格中的对称性破缺。a、DA1-K和DA1-VK水溶液在芳香区的圆二色光谱放大图(上)。图1e的紫外-可见吸收数据放大图作为对比添加(下)。b、DA1-VK干燥样品的双光子共聚焦显微镜图像。图i-iii对应检测器1(380-450 nm检测窗口),图iv-vi对应检测器2(470-550 nm检测窗口);图i和iv对应850 nm激发(仅能被检测器1成像),图ii和v对应920 nm激发(无法被这两个检测器成像),图iii和vi对应950 nm激发(仅能被检测器2成像)。c、d、含1当量NaOH的DA1水溶液(黑色迹线)、DA1-K(蓝色迹线)、DA1-VK(绿色迹线)和DA1-VKVK(橙色迹线)的红外吸收光谱。亚胺区的放大图显示DA1-VKVK中电荷转移相互作用减弱(d)。e、f、DFT优化结构显示DA1(e)和DA1-VK(f)中四个分子簇内的π-π堆积距离(单位Å)。
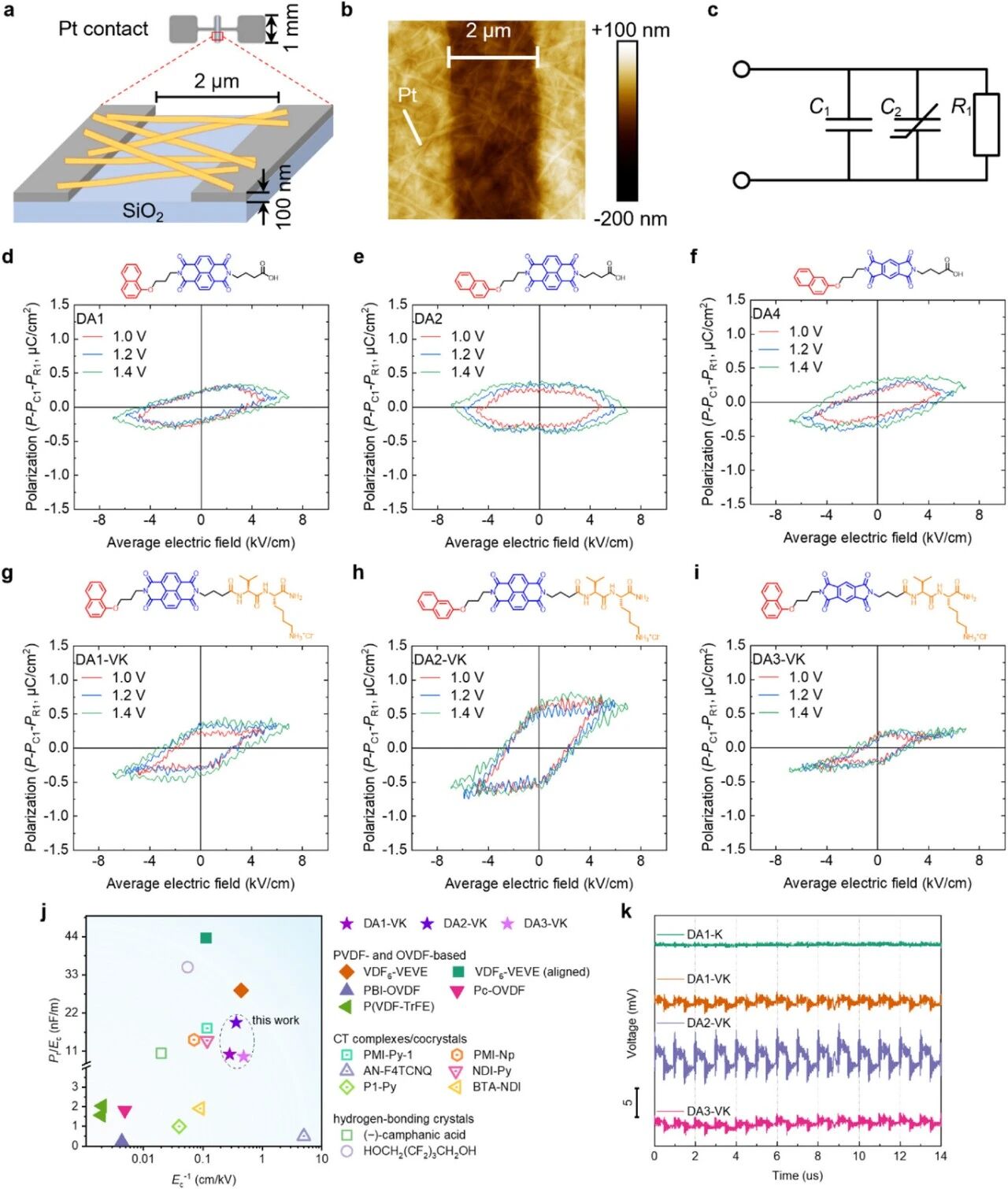
供体-受体肽类两亲分子纳米结构中的铁电性。a、铁电测试装置示意图。b、测试芯片上DA2-VK涂层的原子力显微镜图像。c、被测样品的等效电路图,包含与非线性电容器C2和电阻器R1并联的线性电容器C1。d-i、DA1(d)、DA2(e)、DA4(f)、DA1-VK(g)、DA2-VK(h)和DA3-VK(i)的P-E回线及相应分子结构示意图。j、铁电性DA-PA组装体与其他无金属室温有机铁电体的Pr/Ec与Ec−1关系对比(Pr和Ec数值及缩写定义见表S2)。k、超声刺激下DA-PA样品的压电电压波形(快速傅里叶变换分析见图S43)。(k)中电压曲线为清晰起见已垂直偏移。
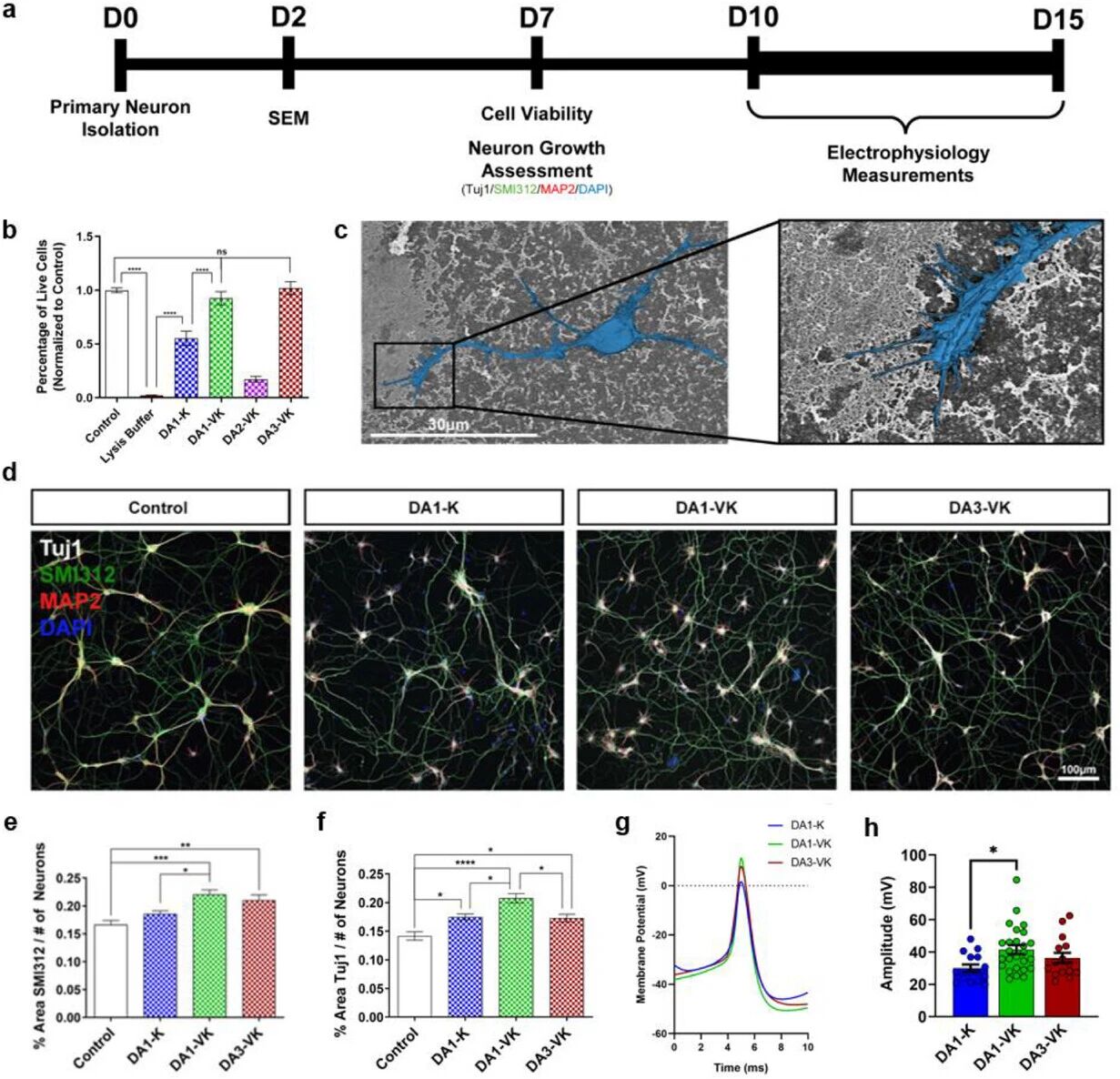
供体-受体肽两亲性纳米结构涂层支持原代皮层神经元存活与生长。a、神经元实验时间线示意图。b、原代神经元在DA-PA材料涂层培养一周后活细胞与总细胞比率(相对于对照组标准化)。活/死细胞可视化结果见图S48。c、在DA3-VK涂层培养48小时的原代神经元(伪彩标注为蓝色)扫描电镜典型显微图像。d、DA-PA涂层培养一周神经元的典型共聚焦图像。原代神经元分别用Tuj1(神经骨架,白色)、MAP2(成熟树突,红色)、SMI312(成熟轴突,绿色)和DAPI(细胞核,蓝色)染色(采用PDL涂层对照)。e、每视野SMI312阳性神经突覆盖面积百分比(经DAPI阳性细胞核数量标准化)定量。f、每视野Tuj1阳性神经突覆盖面积百分比(经DAPI阳性细胞核数量标准化)定量。g、DA-PA涂层培养10-15天神经元的典型动作电位轨迹。h、DA-PA涂层培养10-15天神经元动作电位幅度定量。对于(b、e、f、h)采用单因素方差分析结合Tukey多重比较检验(α=0.05):(*) p < 0.05,(**) p < 0.01,(***) p < 0.001,(****) p < 0.0001。
总结
一项有望推动神经修复的前沿发现 想象一下,有一种材料,它不仅柔软、 biocompatible(生物相容),还能在水中自发组装成有序的纳米结构,并产生稳定的电极化特性。这听起来像是科幻小说,但正是美国西北大学Samuel I. Stupp教授团队最新发表于《Advanced Materials》的研究。他们成功开发出一类新型的“供体-受体肽 amphiphile”分子,能在水中自组装成纳米带,并展现出有趣的铁电性能。关键在于,他们巧妙地利用了肽的手性来打破分子堆砌的对称性,从而在原本可能对称排列的电荷转移体系中诱导出了铁电性。
更令人兴奋的是,这种材料并不仅仅是一项物理化学的杰作。研究团队将小鼠的原代皮层神经元培养在这种铁电纳米材料涂层上,发现了显著的生物学效应。相比于对照组,生长在具有铁电性材料上的神经元,其轴突生长更为发达,神经网络面积更大。进一步的电生理实验表明,这些神经元的动作电位幅度更高,显示出更成熟的电生理功能。研究者推测,这可能是由于铁电材料表面的自发极化能够吸附并形成生物活性分子(如神经营养因子)或离子的浓度梯度,从而模拟体内的微环境,引导和促进神经元的成熟。这项研究不仅为设计新型、可水加工的有机铁电材料提供了新思路,也为开发无需外部电源、能主动与生物系统相互作用的神经修复材料和生物电子器件开辟了诱人的前景。
参考文献:
DOI: 10.1002/adma.202514940
点击下方链接,可直接跳转文献
- 上一款: Advanced Materials | 一
- 下一款: ACS Nano | 通过靶向 siRNA-


 mxene 学术专题
mxene 学术专题