Advanced Materials | 自我扩增纳米医学使溶酶体受阻增强胰管腺癌的饥饿治疗
QQ学术交流群:1092348845
详细介绍
我们提出了一种级联代谢阻滞策略,用于克服 PDAC 饥饿治疗中的适应性代谢代偿。一种缺氧响应纳米医学被设计用于自我放大传递葡萄糖氧化酶(GOx)以消耗葡萄糖和氯喹(CQ)以抑制溶酶体介导的代谢代偿。结合仿生肿瘤靶向载体,该系统破坏代谢可塑性,放大生物能量应激,并为糖酵解成瘾恶性肿瘤提供可转化的框架。

该研究以题为“Self-Amplified Nanomedicine Enables Lysosomal Blockade to Potentiate Starvation Therapy of Pancreatic Ductal Adenocarcinoma”发表在Advanced Materials 上。
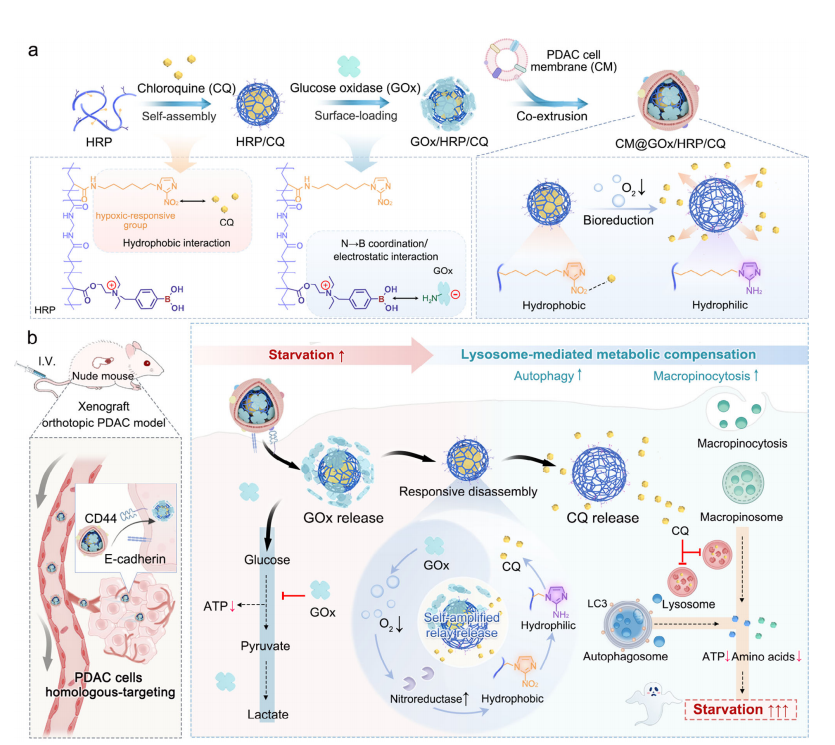
CM@GOx/ HRP /CQ破坏 PDAC 代谢通路的示意图。a) CM@GOx/ HRP /CQ制备工艺示意图。 HRP 通过疏水相互作用共载CQ,通过氮硼酸配位和静电相互作用共载GOx,随后用 PDAC 来源的细胞膜包被以获得CM@GOx/ HRP /CQ。b) 肿瘤积聚后,CM@GOx/ HRP /CQ引发GOx和CQ的自放大接力释放,其中GOx诱导的葡萄糖剥夺引发代谢应激,随后的CQ释放阻断溶酶体介导的代谢补偿,从而破坏 PDAC 代谢通路。
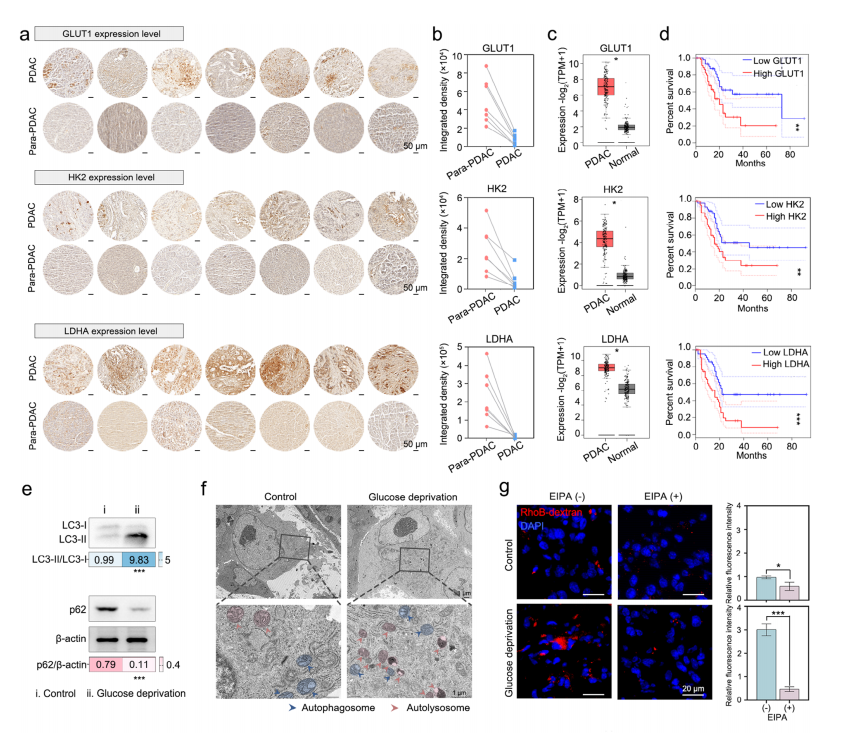
PDAC 中的糖酵解依赖与适应性代谢代偿。a) PDAC 患者肿瘤组织及邻近正常组织(PDAC 旁)中糖酵解相关酶(GLUT1、HK2、 LDHA)的代表性 IHC 染色。比例尺=50 µm 。b) IHC 染色定量分析(n=7)。c) TCGA 数据库中 PDAC 患者糖酵解相关基因的表达水平。d) 根据 TCGA 队列中糖酵解相关基因高/低表达水平分层的 PDAC 患者Kaplan-Meier生存分析。e) 正常喂养(对照组)或12小时禁食(葡萄糖剥夺)后荷 PDAC 小鼠LC3与p62的Western blot分析。f) 正常喂养(对照组)或12小时禁食(葡萄糖剥夺)后荷 PDAC 小鼠肿瘤切片中自噬泡的TEM图像。比例尺=1 µm 。g) 正常喂养(对照组)或12小时禁食(葡萄糖剥夺)后荷 PDAC 小鼠肿瘤组织中 CLSM 图像及RhoB-葡聚糖摄取实验评估的巨胞饮作用。比例尺=20 µm 。数据以均值±标准差表示。*P<0.05,**P<0.01,***P<0.001。
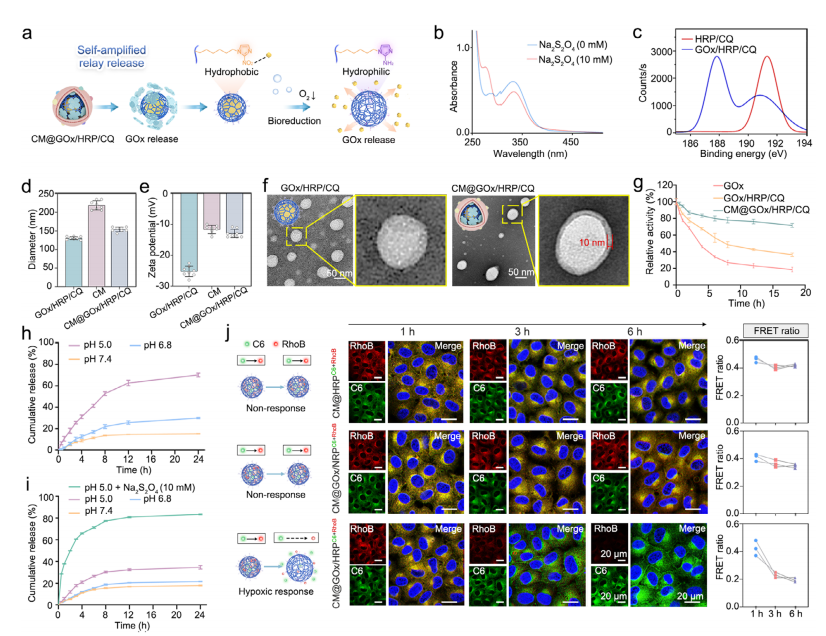
低氧响应性CM@GOx/ HRP /CQ的制备与表征。a) GOx和CQ在 PDAC 中自我放大传递以阻断葡萄糖成瘾和溶酶体依赖性适应性代谢补偿级联的示意图。b) HRP 在与或不与Na2S2O4(10 µm)孵育4小时后的紫外-可见吸收光谱。c) HRP /CQ和GOx/ HRP /CQ的 XPS 分析。d) 通过动态光散射测量的GOx/ HRP /CQ、CM和CM@GOx/ HRP /CQ的直径。e) GOx/ HRP /CQ、CM和CM@GOx/ HRP /CQ的Zeta电位。f) GOx/ HRP /CQ和CM@GOx/ HRP /CQ的TEM图像。比例尺 = 50 nm。g) 10% FBS(生理条件模拟)中游离GOx、GOx/ HRP /CQ和CM@GOx/ HRP /CQ的时间依赖性相对酶活性,归一化至初始值(100%)(n = 5)。h) 不同条件下CM@GOx/ HRP /CQ中GOx的体外释放曲线(n = 3)。i) 不同条件下CM@GOx/ HRP /CQ中CQ的体外释放行为(n = 3)。j) 用CM@ HRP /CQC6+RhoB、CM@GOx/ NRP /CQC6+RhoB、CM@GOx/ HRP /CQC6+RhoB处理的PANC-1细胞的FRET动力学图像和荧光比分析。荧光信号:C6(绿色),RhoB(红色)。比例尺 = 20 µm 。数据以均值 ± 标准差表示。
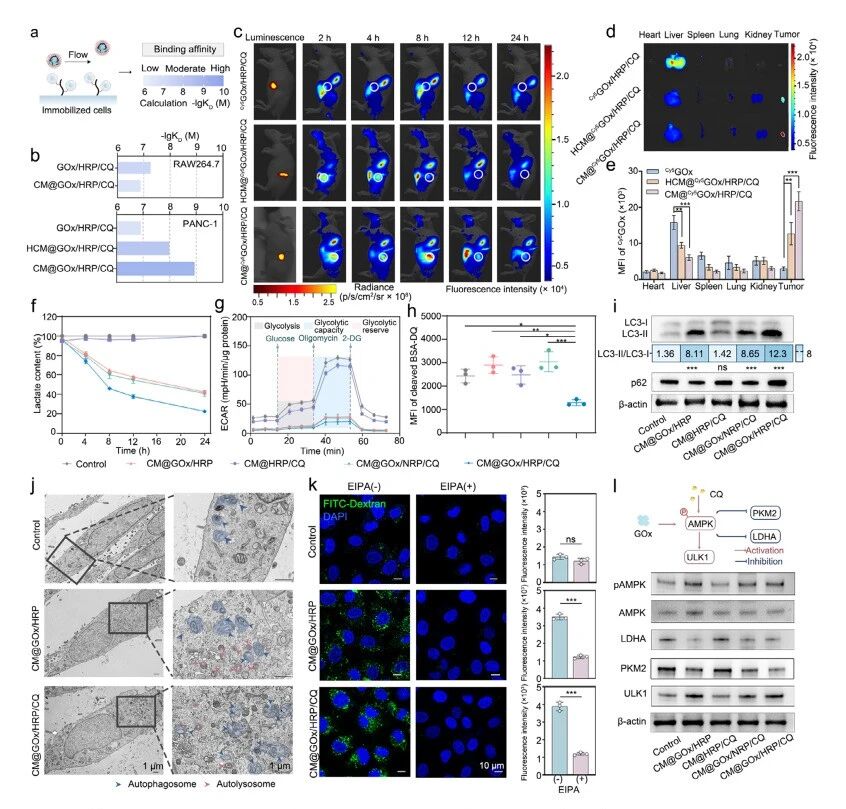
CM@GOx/ HRP /CQ的肿瘤靶向能力及级联代谢阻断机制。a) SPR分析示意图:将RAW264.7或PANC-1细胞固定于LIP-1传感器芯片上,随后注射不同纳米药物以评估结合亲和力。b) 不同纳米药物与RAW264.7或PANC-1细胞的结合亲和力。KD值采用1:1朗缪尔结合模型计算(n=4)。c) 通过Cy5通道分别在不同时间点对静脉注射Cy5GOx/ HRP /CQ、 HCM @Cy5GOx/ HRP /CQ及CM@Cy5GOx/ HRP /CQ的 PDAC 小鼠进行体内荧光成像。在初始时间点同步捕获BLI以定位原位Luc-PANC-1肿瘤。d) 注射Cy5GOx/ HRP /CQ、 HCM @Cy5GOx/ HRP /CQ和CM@Cy5GOx/ HRP /CQ后8小时,从携带 PDAC 的小鼠体内获取主要器官和肿瘤组织的Cy5通道离体荧光图像。e) 注射后8小时获取的主要器官和肿瘤组织中Cy5荧光强度的定量分析(n=3)。f) 经PBS(对照组)、CM@GOx/ HRP 、CM@ HRP /CQ、CM@GOx/ NRP /CQ和CM@GOx/ HRP /CQ处理0、4、8、12和24小时的PANC-1细胞胞外乳酸含量(n=5)。g) 经PBS(对照组)、CM@GOx/ HRP 、CM@ HRP /CQ、CM@GOx/ NRP /CQ和CM@GOx/ HRP /CQ处理的PANC-1细胞 ECAR 曲线,通过葡萄糖、寡霉素和2-脱氧-D-葡萄糖(2-DG)的序贯注射测定(n=5)。
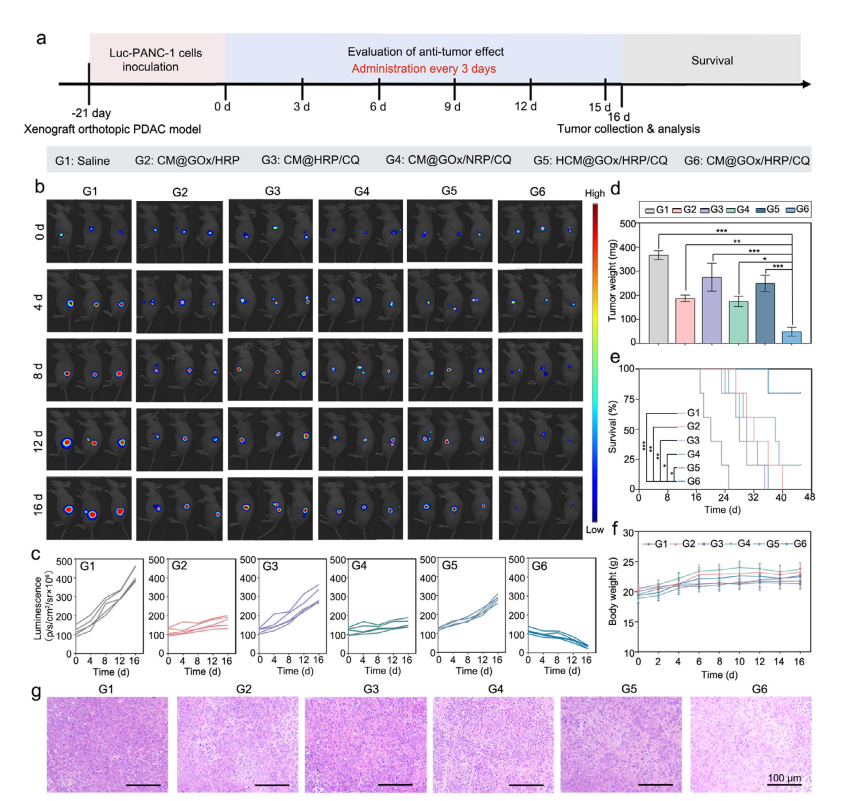
CM@GOx/ HRP /CQ在异种移植原位 PDAC 模型中的体内抗肿瘤效果。a) 异种移植原位 PDAC 模型建立及治疗监测方案示意图。b) 治疗后第0、4、8、12和16天 PDAC 荷瘤小鼠的体内生物发光成像(BLI),可视化不同制剂(包括生理盐水、CM@GOx/ HRP 、CM@ HRP /CQ、CM@GOx/ NRP /CQ、 HCM @GOx/ HRP /CQ和CM@GOx/ HRP /CQ)的肿瘤负荷。c) 胰腺部位生物发光强度的半定量分析随时间变化(n=5)。d) 最终治疗后第16天的肿瘤重量(n=3)。e) PDAC 荷瘤小鼠45天观察期内的Kaplan-Meier生存曲线(n=5)。f) PDAC 荷瘤小鼠在16天给药期间的体重变化(n=5)。g) 治疗结束时采集的肿瘤组织H&E染色结果。比例尺=100 µm 。数据以均值±标准差表示,*p<0.05,**p<0.01,***p<0.001。
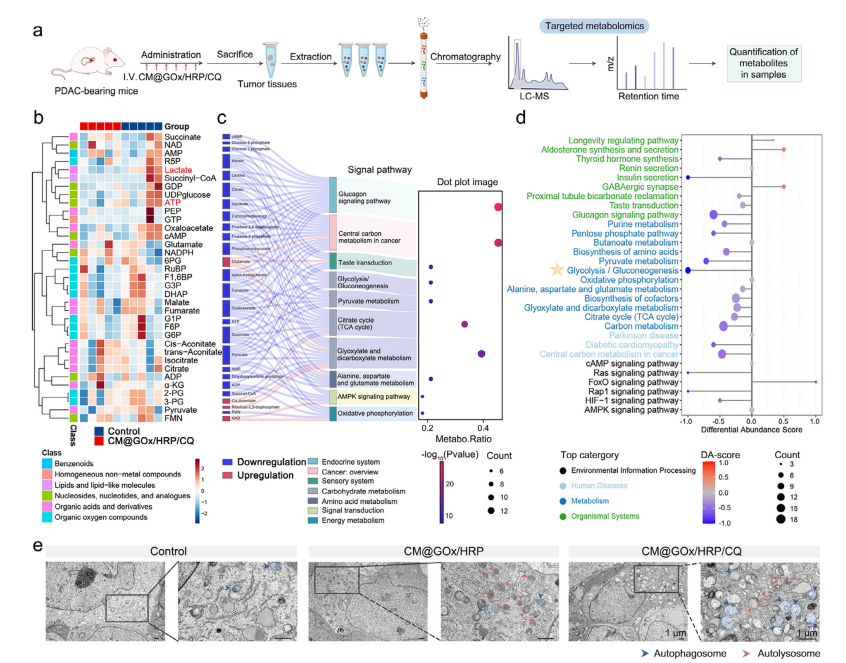
异种移植原位 PDAC 模型中CM@GOx/ HRP /CQ治疗后的代谢组学分析与自噬水平评估。a) 基于LC-MS的靶向代谢组学工作流程示意图。b) 经生理盐水(对照组)或CM@GOx/ HRP /CQ处理的荷瘤小鼠肿瘤组织中靶向代谢物的热图。数据经Z分数标准化(n=5)。c) 对照组与CM@GOx/ HRP /CQ组差异代谢物的通路富集分析,鉴定出10条显著富集的代谢通路,包括糖酵解/糖异生、丙酮酸代谢、三羧酸循环等。d) 显著富集代谢通路的DA分数分析。e) 分别经生理盐水(对照组)、CM@GOx/ HRP 及CM@GOx/ HRP /CQ处理的荷瘤肿瘤中自噬超微结构的透射电镜图像。自噬体特征为完整的胞质内容物与双层膜结构(蓝色箭头),自噬溶酶体则呈现降解内容物与单层膜结构(粉色箭头)。比例尺=1 µm
总结
这篇研究报道了一种针对胰腺导管腺癌(PDAC)的新型自我放大纳米药物CM@GOx/HRP/CQ。该药物采用同源细胞膜伪装,能够主动靶向肿瘤并在缺氧环境下实现级联释放:先释放葡萄糖氧化酶GOx消耗葡萄糖、加剧缺氧,再触发氯喹CQ的爆发释放,从而阻断溶酶体依赖的营养回收通路。实验结果表明,该纳米药物在PDAC原位模型中表现出9.75倍的肿瘤富集增强、92.8%的肿瘤抑制率以及80%的生存率提升,且具有良好的生物安全性。
该研究不仅揭示了PDAC在葡萄糖剥夺下通过溶酶体介导的自噬和大胞饮作用进行代谢补偿的机制,更为临床提供了一种可转化的纳米平台,能够协同抑制糖代谢与溶酶体功能,有望增强PDAC及其他代谢依赖型肿瘤的饥饿治疗效果。
参考文献:
DOI: 10.1002/adma.202519523
点击阅读原文,即可跳转原文链接
- 上一款: Advanced Materials | 从
- 下一款: ACS Nano | 通过靶向 siRNA-


 mxene 学术专题
mxene 学术专题