
咨询热线:
17715390137
18101240246
18914047343
邮件:mxenes@163.com
扫码关注或微信搜索公众号:
二维材料Fronrier
关注后点击右下角联系我们,
进入企业微信。
专业服务在线

本文精选
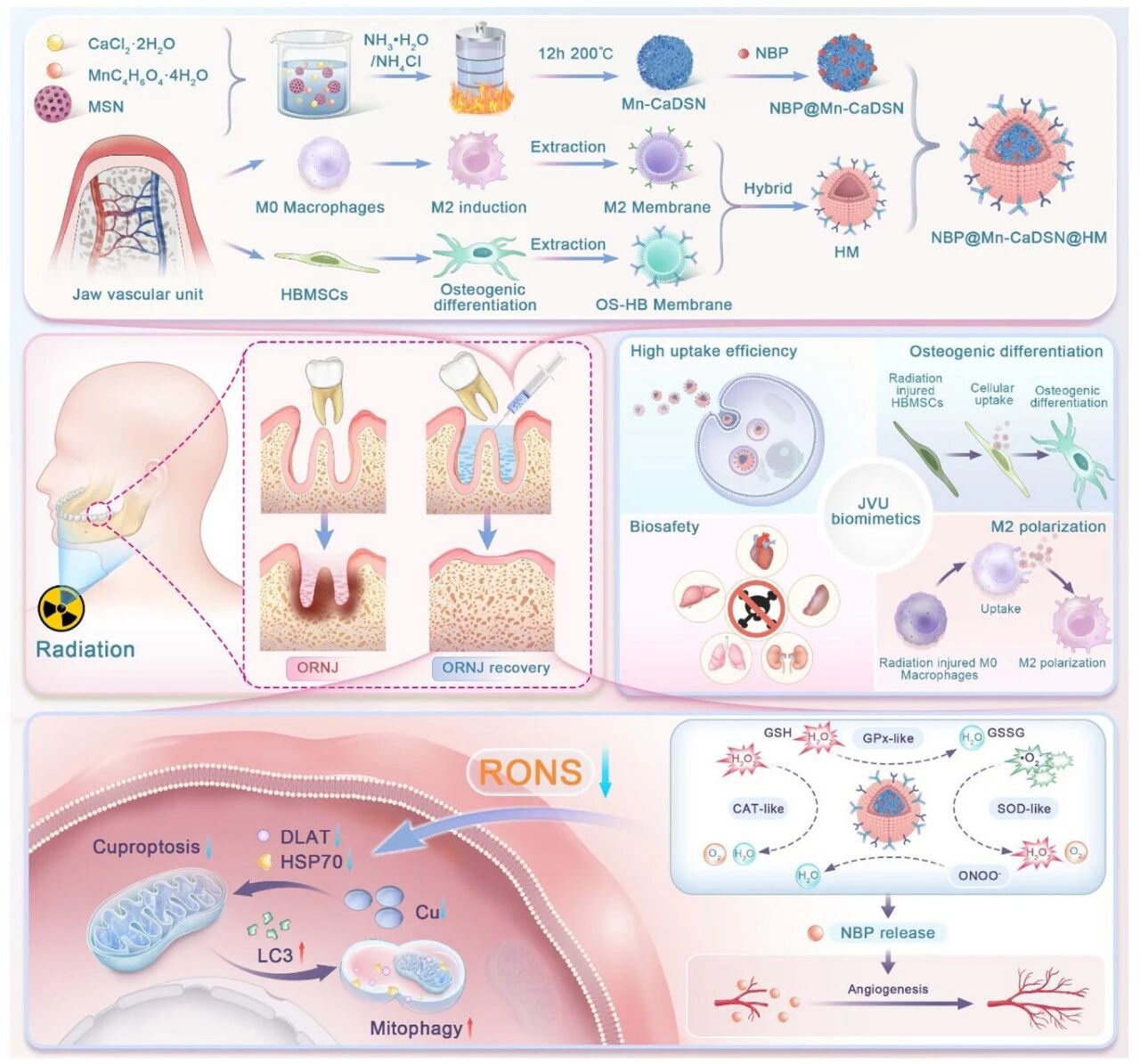
颌骨放射性坏死 (ORNJ) 会导致使人衰弱的并发症,而目前的疗法有组织损伤和血管功能不全的风险。在此,通过用来自 M2 巨噬细胞和成骨诱导的人骨髓间充质干细胞 (HBMSCs) 的杂化膜 (HM) 涂覆 Mn/Ca 双原子位点纳米酶 (Mn-CaDSN) 来开发颌骨血管单位 (JVU)仿生纳米酶。Mn-CaDSN 表现出协同的超氧化物歧化酶样、过氧化氢酶样和谷胱甘肽过氧化物酶(GPx)样活性,Mn-CaDSN 的最大 GPx 样催化活性比 Mn 单原子对照高 2.1 倍。密度泛函理论计算表明,Ca 位点通过 d 波段中心调制优化了底物吸附和 O─H 键裂解。HM 涂层能够靶向 JVU 递送,增强细胞摄取并重新编程辐照的巨噬细胞,使其达到 M2 极化和成骨分化。在辐照细胞中,纳米酶同时消除活性氧/氮(RONS),激活线粒体自噬,并抑制 cuproptos。负载的 Dl-3-n-丁基邻苯酞 (NBP) 进一步增强体内血管生成。在大鼠 ORNJ 模型中,NBP@Mn-CaDSN@HM 通过重新平衡免疫-血管-成骨微环境促进粘膜愈合并增加骨体积分数。这项工作建立了与双原子纳米酶相结合的 JVU 仿生学范式,用于综合 ORNJ 治疗。
创新点
1.本研究突破了传统单原子纳米酶的活性局限,首次构建了锰/钙双原子位点纳米酶(Mn-CaDSN),通过原子级精准排列实现了超氧化物歧化酶、过氧化氢酶与谷胱甘肽过氧化物酶的三重仿生催化活性协同,其谷胱甘肽过氧化物酶样活性达到锰单原子体系的2.1倍,这为设计具有高效级联抗氧化功能的纳米酶提供了全新的分子工程思路。
2. 研究首次将密度泛函理论计算深度融入双原子纳米酶的机理解析,阐明钙位点通过调控d波段中心以优化反应底物吸附能并降低O─H键裂解能垒的电子机制,从而在原子尺度上建立了金属配位环境与酶促活性之间的构效关系,推动了纳米酶设计从经验探索向理性计算的范式转变。
3. 创新性地采用M2巨噬细胞与成骨诱导间充质干细胞的杂化膜(HM)进行仿生涂层修饰,不仅实现了纳米酶对颌骨血管单位的高选择性靶向与递送,更赋予其主动调节辐照后免疫微环境的能力,通过重编程巨噬细胞向M2表型极化并促进成骨分化,实现了“靶向-调控-修复”的一体化治疗功能集成。
原文链接
Diatomic Mn/Ca Nanozymes with Jaw Vascular Unit Mimicry for Triple-Enzyme Synergistic Therapy of Osteoradionecrosis
Advanced Materials ( IF 26.8 )
Pub Date : 2025-11-14
DOI: 10.1002/adma.202517968
Ziyu Chen, Junlin Wang, Yuhao Ruan, Jikang Cao, Huijun Jiang, Jiandong Jiang, Fan Wu, Shuilin Wu, Yuli Wang
 |
 |
 |
 |
| 二维材料Frontier | 生物纳米材料前沿 | MXenes Frontier | 纳米医学Frontier |
|
版权所有 © 2019 北京北科新材科技有限公司
All rights reserved. 京ICP备16054715号-2 |
扫一扫